Anilin Có Công Thức Là Gì? Khám Phá Từ A Đến Z Về Hợp Chất Hóa Học Này

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Anilin, một hợp chất amin thơm quan trọng trong ngành hóa học hữu cơ, thường khơi gợi sự tò mò về cấu trúc và tính chất của nó. Vậy anilin có công thức là gì và điều gì làm nên những đặc điểm nổi bật của nó? Bài viết này sẽ đi sâu khám phá mọi khía cạnh, từ công thức hóa học đến ứng dụng thực tiễn và những lưu ý an toàn khi tiếp xúc với anilin, giúp bạn có cái nhìn toàn diện nhất.
Anilin Có Công Thức Là: Phân Tích Cấu Trúc Hóa Học
Khi nhắc đến anilin, câu hỏi đầu tiên thường xuất hiện là anilin có công thức là gì. Câu trả lời chính xác là Anilin có công thức hóa học là C6H5NH2.
Để hiểu rõ hơn về công thức này, chúng ta có thể phân tích cấu trúc của nó:
- Nhóm Phenyl (-C6H5): Đây là một vòng benzen (C6H6) đã mất đi một nguyên tử hydro. Vòng benzen là một cấu trúc vòng phẳng, bền vững, tạo nên đặc tính "thơm" của anilin.
- Nhóm Amino (-NH2): Đây là nhóm chức amin. Trong anilin, nhóm amino này được gắn trực tiếp vào vòng benzen. Sự tương tác giữa nhóm amino và vòng benzen là yếu tố then chốt quyết định tính chất hóa học đặc trưng của anilin, đặc biệt là tính bazơ yếu của nó.
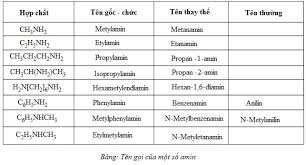
Ngoài tên gọi anilin, hợp chất này còn được biết đến với các tên gọi khác như Phenylamin hoặc Benzenamin. Những tên gọi này đều phản ánh cấu trúc cơ bản của nó: một nhóm amino gắn vào một vòng benzen.
Theo Giáo sư Nguyễn Văn A, chuyên gia Hóa hữu cơ tại Đại học Bách khoa, "Cấu trúc đơn giản nhưng độc đáo của anilin, nơi nhóm amino tương tác trực tiếp với vòng thơm, đã biến nó thành một hợp chất nghiên cứu thú vị và có giá trị ứng dụng cao."
Tính Chất Đặc Trưng Của Anilin (Phenylamin)
Sau khi nắm rõ anilin có công thức là C6H5NH2, việc tìm hiểu về tính chất của nó sẽ giúp chúng ta hiểu sâu hơn về tiềm năng và rủi ro của hợp chất này.
1. Tính Chất Vật Lý
- Trạng thái và màu sắc: Anilin là một chất lỏng không màu ở nhiệt độ phòng. Tuy nhiên, nó dễ dàng bị oxy hóa trong không khí, đặc biệt là dưới tác dụng của ánh sáng, tạo thành các sản phẩm có màu vàng, nâu hoặc đỏ.
- Mùi: Anilin có mùi đặc trưng, hơi hăng và khó chịu.
- Độ tan: Anilin ít tan trong nước lạnh nhưng tan tốt hơn trong nước nóng và tan vô hạn trong nhiều dung môi hữu cơ như ethanol, ether, benzen, v.v.
- Nhiệt độ sôi: Khoảng 184 °C.
- Khối lượng riêng: Khoảng 1.02 g/cm3 (nặng hơn nước).
2. Tính Chất Hóa Học Đáng Chú Ý
Anilin thể hiện cả tính bazơ của nhóm amin và tính chất của vòng benzen, nhưng có những điểm đặc biệt do sự ảnh hưởng lẫn nhau giữa hai nhóm này.
2.1. Tính Bazơ Yếu Của Anilin
Mặc dù là một amin, anilin lại có tính bazơ yếu hơn so với amoniac (NH3) và các amin béo (ví dụ: metylamin). Điều này được giải thích là do hiệu ứng hút electron của vòng benzen:
- Vòng benzen là nhóm hút electron.
- Nó làm giảm mật độ electron trên nguyên tử nitơ của nhóm -NH2.
- Điều này khiến cặp electron không liên kết trên nguyên tử nitơ trở nên kém sẵn sàng hơn để nhận proton (H+).
Do đó, anilin không làm quỳ tím chuyển màu và chỉ tác dụng với các axit mạnh để tạo muối:
C6H5NH2 (anilin) + HCl (axit clohidric) → C6H5NH3Cl (phenylamoni clorua)
2.2. Phản Ứng Thế Vào Vòng Benzen
Nhóm amino (-NH2) là nhóm đẩy electron và hoạt hóa vòng benzen, làm cho các phản ứng thế electrophin vào vòng benzen của anilin xảy ra dễ dàng hơn nhiều so với benzen.
Phản ứng với dung dịch Brom (Phản ứng thế H ở vòng benzen):
Anilin phản ứng rất mạnh với dung dịch brom ở nhiệt độ phòng, tạo kết tủa trắng của 2,4,6-tribromoanilin. Đây là một phản ứng đặc trưng thường dùng để nhận biết anilin.
C6H5NH2 + 3Br2 → C6H2Br3NH2↓ + 3HBr
(2,4,6-tribromoanilin)
Phản ứng với HNO3 đặc: Anilin cũng có thể tham gia phản ứng nitrat hóa.
2.3. Các Phản Ứng Khác
- Phản ứng với axit nitrơ (HNO2): Anilin phản ứng với axit nitrơ ở nhiệt độ thấp (0-5 °C) để tạo muối diazoni, một hợp chất trung gian quan trọng trong tổng hợp hữu cơ, đặc biệt là trong công nghiệp thuốc nhuộm.
- Phản ứng đốt cháy: Anilin cháy trong không khí tạo ra CO2, H2O và N2.
Anilin Được Điều Chế Như Thế Nào?
Trong công nghiệp, anilin chủ yếu được sản xuất thông qua quá trình khử nitrobenzen. Đây là phương pháp phổ biến và kinh tế nhất.
Quá trình điều chế anilin công nghiệp:
Nitrobenzen (C6H5NO2) được điều chế từ benzen và axit nitric. Sau đó, nitrobenzen được khử bằng hydro có xúc tác (như niken, palladium, hoặc platin) hoặc bằng sắt và axit clohidric.
C6H5NO2 + 3H2 (xúc tác Ni, Pd, Pt) → C6H5NH2 + 2H2O
Hoặc:
4C6H5NO2 + 9Fe + 4H2O (HCl) → 4C6H5NH2 + 3Fe3O4
Quy trình này hiệu quả và cho phép sản xuất anilin với số lượng lớn để đáp ứng nhu cầu công nghiệp.
Ứng Dụng Rộng Rãi Của Anilin Trong Đời Sống và Công Nghiệp
Dù anilin có công thức là C6H5NH2 đơn giản, nhưng ứng dụng của nó lại vô cùng đa dạng và quan trọng trong nhiều ngành công nghiệp khác nhau. Anilin đóng vai trò là một nguyên liệu trung gian then chốt.
- Công nghiệp Thuốc Nhuộm: Đây có lẽ là ứng dụng nổi tiếng nhất của anilin. Anilin là tiền chất để sản xuất nhiều loại thuốc nhuộm azo, thuốc nhuộm lưu huỳnh, và thuốc nhuộm indigoid. Ví dụ điển hình là màu chàm (indigo) và anilin đen (aniline black).
- Sản xuất Hóa chất Cao su: Anilin được sử dụng để tổng hợp các chất chống oxy hóa, chất tăng tốc lưu hóa và các hóa chất khác giúp cải thiện tính chất và tuổi thọ của cao su.
- Công nghiệp Dược phẩm: Nhiều loại thuốc và dược chất được tổng hợp từ anilin hoặc các dẫn xuất của nó, bao gồm một số thuốc giảm đau, hạ sốt.
- Chất diệt cỏ và Thuốc trừ sâu: Một số hóa chất nông nghiệp, bao gồm các loại thuốc diệt cỏ và thuốc trừ sâu, cũng có anilin là thành phần trung gian.
- Sản xuất Polymer và Nhựa: Anilin là nguyên liệu chính để sản xuất methylenedianiline (MDA), một tiền chất quan trọng cho diisocyanate (MDI) được dùng trong sản xuất polyurethane – một loại polymer có nhiều ứng dụng từ bọt xốp cách nhiệt đến sợi tổng hợp.
- Sản xuất chất nổ: Một số hợp chất nổ cũng có thể được tổng hợp từ anilin.
Cảnh Báo Về An Toàn Khi Tiếp Xúc Với Anilin
Mặc dù anilin có công thức là C6H5NH2 và có nhiều ứng dụng quan trọng, nhưng nó là một chất độc hại và cần được xử lý hết sức cẩn thận. Hiểu rõ các mối nguy hiểm là cực kỳ cần thiết để đảm bảo an toàn.
-
Độc tính cấp tính: Anilin là chất độc mạnh, có thể hấp thụ qua da, đường hô hấp (hít phải hơi) hoặc đường tiêu hóa (nuốt phải).
- Ảnh hưởng đến máu: Nguy hiểm nhất là anilin gây ra methemoglobin huyết. Methemoglobin là một dạng hemoglobin không thể vận chuyển oxy, dẫn đến tình trạng thiếu oxy trong máu, gây xanh tím môi và móng tay, đau đầu, chóng mặt, buồn nôn, và trong trường hợp nặng có thể gây suy hô hấp, hôn mê và tử vong.
- Ảnh hưởng đến hệ thần kinh: Gây chóng mặt, đau đầu, co giật.
- Kích ứng: Gây kích ứng da, mắt và đường hô hấp.
- Độc tính mãn tính: Tiếp xúc lâu dài với anilin có thể gây tổn thương gan, thận và bàng quang. Anilin cũng được coi là chất có khả năng gây ung thư (carcinogen), đặc biệt là ung thư bàng quang.
Biện pháp phòng ngừa an toàn:
Khi làm việc với anilin, cần tuân thủ nghiêm ngặt các quy tắc an toàn:
- Luôn sử dụng thiết bị bảo hộ cá nhân (PPE) đầy đủ: găng tay chống hóa chất, kính bảo hộ, áo choàng phòng thí nghiệm hoặc quần áo bảo hộ toàn thân.
- Làm việc trong tủ hút hoặc khu vực có hệ thống thông gió tốt để tránh hít phải hơi anilin.
- Tránh tiếp xúc trực tiếp với da, mắt. Nếu bị dính vào da hoặc mắt, cần rửa sạch ngay lập tức với nhiều nước và tìm kiếm sự trợ giúp y tế.
- Không ăn uống hoặc hút thuốc trong khu vực làm việc với anilin.
- Lưu trữ anilin trong các thùng chứa kín, ở nơi khô ráo, thoáng mát, tránh xa ánh sáng trực tiếp và các chất oxy hóa mạnh.
Kết Luận
Qua bài viết này, hy vọng bạn đã có cái nhìn rõ ràng về anilin có công thức là C6H5NH2 và những khía cạnh quan trọng khác của hợp chất này. Anilin là một hợp chất hữu cơ đa năng với cấu trúc đặc biệt, mang lại nhiều ứng dụng giá trị trong công nghiệp từ thuốc nhuộm đến vật liệu polymer.
Tuy nhiên, bên cạnh những lợi ích kinh tế, anilin cũng tiềm ẩn những rủi ro đáng kể về sức khỏe. Việc hiểu rõ tính chất, ứng dụng và đặc biệt là các biện pháp an toàn khi tiếp xúc với anilin là vô cùng cần thiết. Hãy luôn ưu tiên an toàn và kiến thức khoa học để khai thác hiệu quả và bền vững mọi tiềm năng của hóa chất.
Các Câu Hỏi Thường Gặp Về Anilin
Anilin là gì và công thức của nó là gì?
Anilin là amin thơm đơn giản nhất, với công thức hóa học là C6H5NH2. Nó còn được biết đến với tên gọi phenylamin hoặc benzenamin. Anilin là chất lỏng không màu khi tinh khiết, nhưng dễ bị oxy hóa thành màu vàng hoặc nâu khi tiếp xúc với không khí và ánh sáng.
Tại sao anilin lại có tính bazơ yếu hơn amoniac?
Anilin có tính bazơ yếu hơn amoniac là do nhóm phenyl (-C6H5) có hiệu ứng hút electron. Hiệu ứng này làm giảm mật độ electron trên nguyên tử nitơ của nhóm -NH2, khiến cặp electron không liên kết kém sẵn sàng hơn để nhận proton, từ đó làm giảm tính bazơ của anilin.
Anilin có độc không và cách phòng tránh như thế nào?
Có, anilin rất độc hại. Nó có thể hấp thụ qua da, gây methemoglobin huyết (làm giảm khả năng vận chuyển oxy của máu) và tổn thương nội tạng. Để phòng tránh, cần đeo găng tay, kính bảo hộ, khẩu trang, làm việc trong tủ hút và đảm bảo thông gió tốt khi tiếp xúc với anilin.
Anilin được ứng dụng trong những ngành công nghiệp nào?
Anilin có nhiều ứng dụng quan trọng trong công nghiệp, bao gồm sản xuất thuốc nhuộm (như thuốc nhuộm azo), hóa chất cao su, dược phẩm, thuốc trừ sâu và đặc biệt là trong sản xuất polymer như polyurethane thông qua chất trung gian MDI.
Làm thế nào để phân biệt anilin với các amin khác?
Anilin có thể được phân biệt với các amin béo hoặc amoniac bằng phản ứng với dung dịch brom. Anilin sẽ tạo ra kết tủa trắng của 2,4,6-tribromoanilin ngay ở nhiệt độ phòng, một phản ứng rất đặc trưng mà các amin khác thường không có hoặc phản ứng khác biệt.
Có nên tự điều chế anilin tại nhà không?
Tuyệt đối không nên tự điều chế anilin tại nhà. Anilin là một chất độc hại, quá trình tổng hợp đòi hỏi kiến thức chuyên môn sâu, thiết bị an toàn chuyên dụng và khả năng kiểm soát nghiêm ngặt các chất thải. Việc tự ý điều chế có thể gây nguy hiểm nghiêm trọng đến sức khỏe và môi trường.
Khi nào anilin lần đầu tiên được điều chế và xác định công thức?
Anilin lần đầu tiên được phân lập vào năm 1826 bởi Otto Unverdorben từ quá trình chưng cất indigo. Công thức hóa học của anilin được xác định chính xác sau đó, và quá trình tổng hợp công nghiệp từ nitrobenzen đã được phát triển vào giữa thế kỷ 19, mở ra kỷ nguyên mới cho ngành hóa chất hữu cơ.