Bảng tuần hoàn hiện nay không áp dụng nguyên tắc sắp xếp nào sau đây?
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
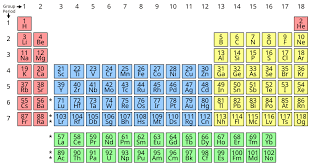
Bảng tuần hoàn các nguyên tố hóa học là một trong những công cụ quan trọng và biểu tượng nhất của khoa học, cung cấp cái nhìn tổng quan về các nguyên tố và mối quan hệ giữa chúng. Từ những nỗ lực đầu tiên của Dmitri Mendeleev cho đến phiên bản hiện đại, bảng tuần hoàn đã trải qua nhiều sự phát triển và cải tiến. Tuy nhiên, có một câu hỏi thường gặp: bảng tuần hoàn hiện nay không áp dụng nguyên tắc sắp xếp nào sau đây? Câu trả lời nằm ở sự thay đổi nền tảng từ một tiêu chí lịch sử sang một tiêu chí khoa học chính xác hơn, giúp giải quyết nhiều bất thường và dự đoán tốt hơn các tính chất hóa học.
Sự Phát Triển Lịch Sử Của Bảng Tuần Hoàn và Nguyên Tắc Sắp Xếp
Trước khi đi sâu vào nguyên tắc không còn được áp dụng, điều quan trọng là phải hiểu hành trình phát triển của bảng tuần hoàn.
Khởi Nguyên Từ Dmitri Mendeleev và Nguyên Tắc Khối Lượng Nguyên Tử
Vào năm 1869, nhà hóa học người Nga Dmitri Mendeleev đã công bố phiên bản đầu tiên của bảng tuần hoàn. Thành công rực rỡ của ông đến từ việc sắp xếp các nguyên tố theo khối lượng nguyên tử tăng dần và đặt chúng vào các cột, hàng dựa trên tính chất hóa học tương tự. Điểm đặc biệt là Mendeleev đã để lại những khoảng trống cho các nguyên tố chưa được khám phá và dự đoán chính xác tính chất của chúng, như germanium, gallium và scandium. Đây là một bước đột phá vĩ đại, cho thấy sự tồn tại của một quy luật tự nhiên trong các nguyên tố.
Mendeleev không chỉ sắp xếp các nguyên tố đã biết mà còn dũng cảm dự đoán sự tồn tại và tính chất của các nguyên tố chưa được khám phá, một minh chứng cho thiên tài của ông.
Tuy nhiên, nguyên tắc sắp xếp theo khối lượng nguyên tử cũng bộc lộ một số bất thường. Ví dụ, teluri (Te) có khối lượng nguyên tử lớn hơn iốt (I), nhưng Mendeleev vẫn đặt teluri trước iốt để đảm bảo iốt nằm cùng nhóm với flo, clo và brom – các halogen có tính chất tương tự. Điều này cho thấy rằng có một yếu tố cơ bản hơn khối lượng nguyên tử đang chi phối tính tuần hoàn của các nguyên tố.
Bảng Tuần Hoàn Hiện Nay Không Áp Dụng Nguyên Tắc Sắp Xếp Nào Sau Đây?
Chính từ những bất thường nhỏ trong bảng của Mendeleev, các nhà khoa học đã tìm kiếm một nền tảng sắp xếp vững chắc hơn. Và đây là câu trả lời chính cho câu hỏi trọng tâm của chúng ta: bảng tuần hoàn hiện nay không áp dụng nguyên tắc sắp xếp theo khối lượng nguyên tử tăng dần làm tiêu chí chính.
Vì Sao Nguyên Tắc Khối Lượng Nguyên Tử Bị Loại Bỏ (Làm Tiêu Chí Chính)?
Nguyên nhân chính dẫn đến sự thay đổi này là khám phá của nhà vật lý người Anh Henry Moseley vào năm 1913. Moseley đã sử dụng kỹ thuật nhiễu xạ tia X để xác định điện tích hạt nhân (số proton) của các nguyên tố. Ông nhận thấy rằng việc sắp xếp các nguyên tố theo số hiệu nguyên tử (Z) tăng dần sẽ giải quyết mọi bất thường mà Mendeleev gặp phải. Cụ thể:
- Khắc phục bất thường: Với số hiệu nguyên tử, teluri (Z=52) tự nhiên đứng trước iốt (Z=53), phù hợp với tính chất hóa học của chúng mà không cần phải "bẻ cong" quy tắc.
- Cơ sở vật lý vững chắc: Số hiệu nguyên tử không chỉ là một con số; nó đại diện cho số proton trong hạt nhân, yếu tố quyết định danh tính của nguyên tố và cấu hình electron của nó.
Kể từ khám phá của Moseley, số hiệu nguyên tử đã trở thành nền tảng không thể lay chuyển của bảng tuần hoàn hiện đại. Vì vậy, khi nói đến việc bảng tuần hoàn hiện nay không áp dụng nguyên tắc sắp xếp nào sau đây, câu trả lời rõ ràng nhất là nguyên tắc dựa hoàn toàn vào khối lượng nguyên tử tăng dần.
Các Nguyên Tắc Đang Áp Dụng Trong Bảng Tuần Hoàn Hiện Nay
Để hiểu rõ hơn về sự khác biệt, hãy cùng điểm qua các nguyên tắc cốt lõi đang định hình bảng tuần hoàn ngày nay:
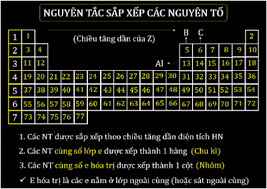
1. Số Hiệu Nguyên Tử (Z) Tăng Dần: Nền Tảng Hiện Đại
Đây là nguyên tắc sắp xếp cơ bản nhất. Mỗi nguyên tố được gán một số hiệu nguyên tử duy nhất, đại diện cho số proton trong hạt nhân của nó. Việc sắp xếp theo số hiệu nguyên tử đảm bảo thứ tự logic và khoa học cho các nguyên tố, từ hydro (Z=1) đến các nguyên tố siêu nặng được tổng hợp gần đây.
2. Cấu Hình Electron và Tính Chất Hóa Học Tương Tự
Mặc dù số hiệu nguyên tử là nguyên tắc chính, bảng tuần hoàn vẫn duy trì tính chất tuần hoàn dựa trên cấu hình electron của nguyên tử. Các nguyên tố có cấu hình electron lớp ngoài cùng tương tự nhau được xếp vào cùng một nhóm (cột dọc). Điều này giải thích tại sao các nguyên tố trong cùng một nhóm lại có tính chất hóa học tương tự nhau (ví dụ: tất cả các kim loại kiềm đều phản ứng mạnh với nước).
- Chu kỳ (hàng ngang): Đại diện cho số lớp electron mà nguyên tử đó có. Khi đi từ trái sang phải trong một chu kỳ, số electron lớp ngoài cùng tăng dần.
- Nhóm (cột dọc): Đại diện cho các nguyên tố có số electron hóa trị (electron lớp ngoài cùng) như nhau, dẫn đến các tính chất hóa học tương tự.
3. Phân Loại Theo Tính Chất (Kim Loại, Phi Kim, Á Kim)
Bảng tuần hoàn hiện đại còn phân loại các nguyên tố dựa trên tính chất chung của chúng thành:
- Kim loại: Chiếm phần lớn bảng tuần hoàn, thường ở bên trái và giữa.
- Phi kim: Nằm ở phía trên bên phải.
- Á kim: Nằm dọc theo đường chéo phân chia kim loại và phi kim, có tính chất trung gian.
Tầm Quan Trọng Của Việc Hiểu Đúng Nguyên Tắc Sắp Xếp Bảng Tuần Hoàn
Việc nắm rõ bảng tuần hoàn hiện nay không áp dụng nguyên tắc sắp xếp nào sau đây và thay vào đó là nguyên tắc nào không chỉ là kiến thức cơ bản trong hóa học mà còn mang ý nghĩa sâu sắc:
- Phản ánh sự tiến bộ khoa học: Nó cho thấy cách khoa học không ngừng phát triển, điều chỉnh và hoàn thiện các mô hình dựa trên bằng chứng mới.
- Hiểu rõ hơn về nguyên tố: Việc sắp xếp theo số hiệu nguyên tử giúp chúng ta hiểu sâu hơn về cấu trúc nguyên tử và cách cấu hình electron quyết định tính chất hóa học.
- Dự đoán và khám phá: Một bảng tuần hoàn được sắp xếp chính xác vẫn là công cụ dự đoán mạnh mẽ, hỗ trợ việc tìm kiếm và tổng hợp các nguyên tố mới.
Kết Luận
Tóm lại, mặc dù khối lượng nguyên tử là nguyên tắc ban đầu giúp Mendeleev tạo ra nền tảng của bảng tuần hoàn, nhưng bảng tuần hoàn hiện nay không áp dụng nguyên tắc sắp xếp theo khối lượng nguyên tử tăng dần làm tiêu chí chính. Thay vào đó, nó dựa vững chắc vào số hiệu nguyên tử (số proton) của mỗi nguyên tố, cùng với cấu hình electron để xác định vị trí nhóm và chu kỳ. Sự chuyển đổi này đánh dấu một bước tiến quan trọng trong sự hiểu biết của chúng ta về vật chất và thế giới hóa học.
Câu Hỏi Thường Gặp (FAQ)
Là gì nguyên tắc chính để sắp xếp bảng tuần hoàn hiện nay?
Nguyên tắc chính để sắp xếp bảng tuần hoàn hiện nay là theo số hiệu nguyên tử (số proton trong hạt nhân) tăng dần của các nguyên tố.
Tại sao khối lượng nguyên tử không còn là nguyên tắc sắp xếp chính?
Khối lượng nguyên tử không còn là nguyên tắc chính vì nó gây ra một số bất thường, ví dụ như trường hợp của teluri và iốt, mà số hiệu nguyên tử của Moseley đã khắc phục hoàn toàn.
Ai là người đã thay đổi nguyên tắc sắp xếp bảng tuần hoàn?
Henry Moseley là nhà khoa học chủ chốt đã thay đổi nguyên tắc sắp xếp bảng tuần hoàn từ khối lượng nguyên tử sang số hiệu nguyên tử vào năm 1913.
Như thế nào việc sắp xếp theo số hiệu nguyên tử giúp ích cho hóa học?
Việc sắp xếp theo số hiệu nguyên tử giúp giải thích các tính chất hóa học tuần hoàn một cách chính xác hơn, vì số proton quyết định cấu hình electron và do đó là tính chất hóa học của nguyên tố.
Bảng tuần hoàn hiện nay không áp dụng nguyên tắc sắp xếp nào sau đây trong các nhóm và chu kỳ?
Trong các nhóm và chu kỳ, bảng tuần hoàn vẫn không áp dụng nguyên tắc sắp xếp dựa trên sự tăng dần của khối lượng nguyên tử làm tiêu chí duy nhất, mà chủ yếu dựa vào số hiệu nguyên tử và cấu hình electron.
Có nên học thuộc lòng bảng tuần hoàn theo khối lượng nguyên tử không?
Không nên học thuộc lòng bảng tuần hoàn theo khối lượng nguyên tử làm tiêu chí chính. Thay vào đó, hãy tập trung vào số hiệu nguyên tử và cách nó liên quan đến vị trí nhóm và chu kỳ để hiểu sâu sắc hơn.