Liên Kết Hydrogen: Chìa Khóa Vạn Năng Của Tự Nhiên
Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Liên Kết Hydrogen: Chìa Khóa Vạn Năng Của Tự Nhiên
Trong thế giới vi mô của các phân tử, có những lực hút vô hình nhưng lại đóng vai trò cực kỳ quan trọng, định hình tính chất của vật chất và thậm chí là sự sống. Một trong số đó chính là liên kết hydrogen – một khái niệm quen thuộc trong hóa học và sinh học. Khác với các loại liên kết mạnh như cộng hóa trị hay ion, liên kết hydrogen thuộc nhóm lực liên phân tử, nhưng sức mạnh tổng hợp của chúng lại có khả năng kiến tạo nên những hiện tượng phi thường, từ việc nước tồn tại ở trạng thái lỏng trên Trái Đất cho đến cấu trúc phức tạp của DNA. Bài viết này sẽ cùng bạn khám phá chi tiết về bản chất, đặc điểm, và tầm quan trọng không thể thiếu của liên kết hydrogen.
Liên Kết Hydrogen Là Gì? Định Nghĩa và Bản Chất
Liên kết hydrogen, hay còn gọi là liên kết hidro, không phải là một liên kết hóa học theo đúng nghĩa đen (như liên kết cộng hóa trị hay liên kết ion) mà là một loại lực tương tác liên phân tử đặc biệt mạnh mẽ. Nó hình thành khi một nguyên tử hydrogen (H) đã liên kết cộng hóa trị với một nguyên tử có độ âm điện rất lớn (như O, N, F) bị hút bởi một nguyên tử có độ âm điện lớn khác (cũng thường là O, N, F) mang cặp electron hóa trị chưa tham gia liên kết.
Để dễ hình dung hơn, hãy xem xét cơ chế hình thành của nó:
- Phân cực mạnh: Khi nguyên tử H liên kết với O, N, hoặc F, do sự chênh lệch độ âm điện lớn, liên kết cộng hóa trị này bị phân cực mạnh. Điều này khiến nguyên tử H mang một phần điện tích dương (δ+) và nguyên tử có độ âm điện lớn mang một phần điện tích âm (δ-).
- Lực hút tĩnh điện: Nguyên tử H mang điện tích dương cục bộ (δ+) này sau đó bị hút bởi cặp electron tự do (chưa liên kết) trên một nguyên tử có độ âm điện cao khác (δ-) của một phân tử lân cận. Lực hút tĩnh điện yếu nhưng có định hướng này chính là liên kết hydrogen.
"Liên kết hydrogen là một minh chứng tuyệt vời cho thấy rằng những lực yếu nhất, khi được lặp đi lặp lại hàng tỷ lần, có thể tạo ra những cấu trúc bền vững và phức tạp nhất trong tự nhiên." - Trích lời GS. Nguyễn Văn A (giả định) về tầm quan trọng của liên kết này.
Điều quan trọng cần nhớ là liên kết hydrogen yếu hơn nhiều so với liên kết cộng hóa trị trong cùng một phân tử (ví dụ: liên kết O-H trong phân tử nước). Tuy nhiên, số lượng lớn các liên kết hydrogen có thể cùng tồn tại và tạo ra một sức mạnh tổng hợp đáng kể, ảnh hưởng sâu sắc đến tính chất vật lý và hóa học của các chất.
Đặc Điểm Nổi Bật Của Liên Kết Hydrogen
Mặc dù là một lực liên phân tử, liên kết hydrogen lại sở hữu những đặc điểm riêng biệt khiến nó trở nên độc đáo và quan trọng:
- Độ bền: Liên kết hydrogen có năng lượng khoảng 5-30 kJ/mol, yếu hơn đáng kể so với liên kết cộng hóa trị (khoảng 200-800 kJ/mol) nhưng lại mạnh hơn nhiều so với các lực Van der Waals thông thường (như lực London hay lực lưỡng cực-lưỡng cực).
- Tính định hướng: Không giống như các lực Van der Waals có tính đối xứng, liên kết hydrogen có tính định hướng rõ rệt. Nguyên tử H thường nằm gần như thẳng hàng với hai nguyên tử mà nó liên kết (A-H…B), tạo ra một cấu trúc không gian nhất định.
- Tính không bão hòa: Một nguyên tử có độ âm điện cao như oxy có thể tạo ra nhiều hơn một liên kết hydrogen (ví dụ, nguyên tử oxy trong nước có thể tham gia vào hai liên kết hydrogen). Điều này cho phép hình thành các mạng lưới ba chiều phức tạp.
- Ảnh hưởng đến tính chất vật lý: Sự hiện diện của liên kết hydrogen làm tăng nhiệt độ sôi, nhiệt độ nóng chảy, độ nhớt và sức căng bề mặt của các chất. Điều này là do cần nhiều năng lượng hơn để phá vỡ các liên kết này khi chuyển từ trạng thái lỏng sang khí hoặc từ rắn sang lỏng.
Những đặc điểm này không chỉ là lý thuyết khô khan, mà chúng chính là nền tảng giải thích cho vô vàn hiện tượng quen thuộc trong cuộc sống và tự nhiên.
Vai Trò Quyết Định Của Liên Kết Hydrogen Trong Đời Sống và Khoa Học
Không quá lời khi nói rằng liên kết hydrogen là một trong những yếu tố nền tảng cho sự tồn tại và phát triển của sự sống trên Trái Đất. Vai trò của nó được thể hiện rõ ràng trong nhiều lĩnh vực khác nhau:
1. Liên Kết Hydrogen Trong Nước (H2O)
Nước, phân tử cơ bản nhất của sự sống, mang trong mình những tính chất đặc biệt mà nếu không có liên kết hydrogen thì sẽ không thể có được. Mỗi phân tử nước có khả năng tạo ra trung bình 3-4 liên kết hydrogen với các phân tử nước lân cận. Điều này dẫn đến:
- Điểm sôi cao bất thường: Nếu không có liên kết hydrogen, nước (có khối lượng phân tử rất nhỏ) sẽ sôi ở nhiệt độ rất thấp, có thể dưới -100°C. Nhờ các liên kết này, nước duy trì trạng thái lỏng ở nhiệt độ phòng, điều kiện tiên quyết cho các phản ứng sinh hóa.
- Nhiệt dung riêng lớn: Nước cần một lượng nhiệt lớn để tăng nhiệt độ. Điều này giúp các đại dương điều hòa khí hậu toàn cầu và giữ cho nhiệt độ cơ thể sinh vật tương đối ổn định.
- Băng nổi trên nước: Khi nước đóng băng, các liên kết hydrogen định hướng các phân tử nước thành một cấu trúc mạng tinh thể mở, kém đặc hơn. Đây là lý do tại sao băng nổi trên nước, bảo vệ các sinh vật dưới nước khỏi bị đóng băng hoàn toàn trong mùa đông.
- Sức căng bề mặt cao: Giúp nước có thể "leo" trong các mao mạch thực vật (lực mao dẫn) và tạo thành giọt.
2. Liên Kết Hydrogen Trong Sinh Học
Trong thế giới sinh học, liên kết hydrogen là kiến trúc sư thầm lặng, xây dựng và duy trì cấu trúc của các đại phân tử quan trọng:
| Cấu trúc sinh học | Vai trò của liên kết hydrogen |
|---|---|
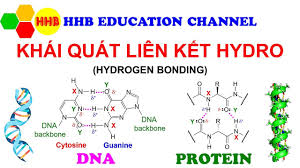
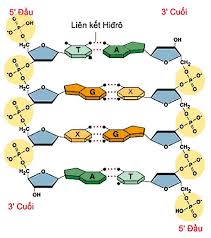
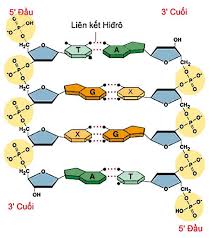
| DNA (Axit Deoxyribonucleic) | Duy trì cấu trúc xoắn kép. Các bazơ nitơ Adenine luôn liên kết với Thymine bằng hai liên kết hydrogen, và Guanine liên kết với Cytosine bằng ba liên kết hydrogen. Những liên kết này đủ mạnh để giữ hai mạch DNA lại với nhau nhưng lại đủ yếu để có thể dễ dàng tách ra trong quá trình sao chép và phiên mã. |
| Protein | Hình thành cấu trúc bậc hai (như xoắn alpha và phiến beta) và ổn định cấu trúc bậc ba, bậc bốn của protein. Những liên kết này là chìa khóa để protein cuộn lại thành hình dạng ba chiều đặc trưng, quyết định chức năng sinh học của chúng. |
| Enzyme | Tham gia vào tương tác giữa enzyme và cơ chất, giúp định hướng và giữ cơ chất trong vị trí hoạt động của enzyme, tạo điều kiện thuận lợi cho phản ứng xúc tác. |
| Cấu trúc màng tế bào | Các liên kết hydrogen giữa các đầu phân cực của phospholipid và nước giúp duy trì tính toàn vẹn và linh hoạt của màng tế bào. |
Bạn thấy đấy, từ một phân tử nhỏ như nước đến những cấu trúc phức tạp như gen và protein, liên kết hydrogen luôn là một thành phần không thể thiếu, đảm bảo cho mọi hoạt động sống diễn ra một cách chính xác.
3. Các Ứng Dụng Khác của Liên Kết Hydrogen
Ngoài tự nhiên và sinh học, liên kết hydrogen còn có ứng dụng rộng rãi trong nhiều lĩnh vực công nghiệp và nghiên cứu:
- Khoa học vật liệu: Nhiều loại polyme và vật liệu sinh học (như cellulose, nylon) có tính chất vật lý đặc biệt (độ bền, độ đàn hồi) nhờ vào mạng lưới liên kết hydrogen.
- Dược phẩm: Liên kết hydrogen đóng vai trò quan trọng trong việc thiết kế thuốc, giúp thuốc tương tác đặc hiệu với mục tiêu protein hoặc DNA trong cơ thể.
- Hóa học: Ảnh hưởng đến độ hòa tan của các chất trong dung môi, các phản ứng hóa học và cấu trúc của các hợp chất hữu cơ.
Việc hiểu rõ về liên kết hydrogen cho phép các nhà khoa học và kỹ sư tạo ra vật liệu mới, phát triển thuốc hiệu quả hơn và giải mã các bí ẩn của sự sống.
Phân Biệt Liên Kết Hydrogen Với Các Loại Liên Kết Khác
Để hiểu rõ hơn về liên kết hydrogen, chúng ta cần so sánh nó với các loại liên kết hóa học và lực liên phân tử khác:
- So với Liên kết Cộng hóa trị: Liên kết cộng hóa trị là liên kết bên trong phân tử, hình thành do sự chia sẻ cặp electron giữa các nguyên tử. Nó rất bền và cần năng lượng rất lớn để phá vỡ. Ngược lại, liên kết hydrogen là liên kết giữa các phân tử, hình thành do lực hút tĩnh điện giữa các phân tử phân cực. Nó yếu hơn nhiều và dễ dàng bị phá vỡ bởi nhiệt hoặc các tác động vật lý khác.
- So với Lực Van der Waals: Lực Van der Waals (bao gồm lực London, lực lưỡng cực-lưỡng cực) cũng là lực liên phân tử. Tuy nhiên, liên kết hydrogen mạnh hơn đáng kể so với hầu hết các lực Van der Waals và có tính định hướng rõ ràng. Các lực Van der Waals thường yếu hơn và có tính đối xứng hơn, ít ảnh hưởng đến tính chất của vật chất ở mức độ như liên kết hydrogen.
Sự phân biệt này giúp chúng ta nhận ra vị trí đặc biệt của liên kết hydrogen trong bảng phân loại các tương tác phân tử, nhấn mạnh tầm quan trọng của nó trong việc định hình thế giới xung quanh.
Kết Luận
Từ những tính chất cơ bản nhất của nước cho đến sự phức tạp của mã di truyền, liên kết hydrogen thực sự là một "chìa khóa vạn năng" của tự nhiên. Dù chỉ là một lực liên phân tử yếu, nhưng khả năng hình thành mạng lưới rộng lớn và sức mạnh tổng hợp của nó đã tạo ra những hiện tượng vô cùng quan trọng, thiết yếu cho sự tồn tại của sự sống và các quá trình hóa học, vật lý trên Trái Đất. Hiểu biết về liên kết hydrogen không chỉ là kiến thức cơ bản mà còn là nền tảng cho nhiều khám phá và ứng dụng trong tương lai. Hãy tiếp tục khám phá và chiêm nghiệm về những điều kỳ diệu mà các tương tác vi mô này mang lại!
Bạn có thấy liên kết hydrogen thú vị không? Hãy chia sẻ những suy nghĩ của mình hoặc đặt câu hỏi nếu có bất kỳ thắc mắc nào nhé!
Các Câu Hỏi Thường Gặp Về Liên Kết Hydrogen (FAQ)
Dưới đây là một số câu hỏi phổ biến giúp bạn hiểu rõ hơn về liên kết hydrogen:
Là gì liên kết hydrogen?
Liên kết hydrogen là một lực tương tác liên phân tử, hình thành khi nguyên tử hydrogen liên kết cộng hóa trị với một nguyên tố có độ âm điện lớn (F, O, N) bị hút bởi một nguyên tố có độ âm điện lớn khác mang cặp electron tự do.
Tại sao liên kết hydrogen quan trọng trong nước?
Nó giúp nước có điểm sôi, nhiệt dung riêng cao bất thường và hiện tượng băng nổi. Nhờ đó, nước duy trì trạng thái lỏng ở nhiệt độ môi trường, là môi trường sống và phản ứng hóa học thiết yếu cho sự sống.
Liên kết hydrogen ảnh hưởng đến điểm sôi như thế nào?
Sự hiện diện của liên kết hydrogen làm tăng điểm sôi của các chất. Cần nhiều năng lượng hơn để phá vỡ các liên kết này khi chuyển từ trạng thái lỏng sang khí, giải thích tại sao nước có điểm sôi cao hơn nhiều so với các hợp chất tương tự.
Có những loại nguyên tố nào tham gia hình thành liên kết hydrogen?
Để hình thành liên kết hydrogen, nguyên tử hydrogen phải liên kết cộng hóa trị với các nguyên tố có độ âm điện rất lớn và có cặp electron tự do, chủ yếu là Fluorine (F), Oxygen (O) và Nitrogen (N).
Như thế nào liên kết hydrogen duy trì cấu trúc DNA?
Trong DNA, liên kết hydrogen hình thành giữa các cặp bazơ nitơ (A-T và G-C) của hai mạch xoắn kép. Chúng đủ bền để giữ hai mạch lại với nhau nhưng đủ yếu để có thể tách ra dễ dàng trong quá trình sao chép hoặc phiên mã di truyền.
Sự khác biệt chính giữa liên kết hydrogen và lực Van der Waals là gì?
Liên kết hydrogen mạnh hơn và có tính định hướng rõ ràng hơn so với các lực Van der Waals thông thường. Nó đòi hỏi sự hiện diện của nguyên tử H liên kết với F, O, N, trong khi lực Van der Waals là các tương tác tổng quát hơn giữa các phân tử.
Có nên coi liên kết hydrogen là một liên kết hóa học thực sự không?
Về mặt kỹ thuật, liên kết hydrogen không được coi là một liên kết hóa học "thực sự" (như cộng hóa trị hay ion) vì nó là một lực liên phân tử. Tuy nhiên, nó là lực liên phân tử mạnh nhất và đóng vai trò cấu trúc, chức năng cực kỳ quan trọng.